電位滴定法檢測牛奶中的還原糖含量——高錳酸鉀法
試樣經除去蛋白質后,其中還原糖把銅鹽還原為氧化亞銅,加硫酸鐵后,氧化亞銅被氧化為銅鹽,經高錳酸鉀溶液滴定氧化作用后生成的亞鐵鹽,根據高錳酸鉀消耗量,計算氧化亞銅含量,再查表得還原糖量。
實驗部分
1.1實驗儀器
HanonT960自動電位滴定儀,鉑復合電極,10ml滴定管單元,常用天平

1.2試劑與溶液
實驗中涉及到的試劑,均為優級純或分析純;實驗用水為三級純凈水。
1.2.1 堿性酒石酸銅甲液:稱取無水硫酸銅11.08448g,加適量水溶解,加硫酸0.25mL,再加水稀釋至250mL;
1.2.2 堿性酒石酸銅乙液:稱取酒石酸鉀鈉86.5g與氫氧化鈉25g,加適量水溶解,并稀釋至250mL,貯存于橡膠塞玻璃瓶內;
1.2.3 氫氧化鈉溶液(40g/L):稱取氫氧化鈉4g,加水溶解并稀釋至100mL;
1.2.4 硫酸鐵溶液(50g/L):稱取硫酸鐵12.5g,加水50mL溶解后,慢慢加入硫酸25mL,冷后加水稀釋至250mL。
1.2.5 高錳酸鉀標準滴定溶液[c(1/5KMnO4)=0.1000mol/L]:稱取0.825g高錳酸鉀,溶于263mL水中,緩緩煮沸15min,冷卻,于暗處放置。
1.3實驗過程
儀器準備,請參照說明書。
1.3.1實驗步驟:
樣品的前處理:稱取試樣25g左右(精確至0.001g),移至250mL容量瓶中,加水50mL,搖勻后加堿性酒石酸銅甲液10mL及氫氧化鈉溶液4mL,加水至刻度,混勻。靜置30min,用干燥濾紙過濾,棄去初濾液,取后續濾液備用。
試樣溶液的測定:
(1)精確吸取處理后的試樣溶液5.0mL于燒杯內,加入堿性酒石酸銅甲液2.5mL及堿性酒石酸銅乙液2.5mL。于燒杯上蓋一表面皿,在預先打開的電爐上加熱,控制在4min內沸騰,再精確煮沸2min。在布氏漏斗上蓋一層濾紙,趁熱抽濾。抽濾時需將溶液沿玻璃棒緩慢傾倒至濾紙上,以防氧化亞銅沿濾紙邊緣流失。
(2)用60℃熱水洗滌燒杯及沉淀至少三次,至洗液不呈堿性為止。將濾紙放回原燒杯,加硫酸鐵溶液20mL,用玻棒攪拌濾紙使附著的氧化亞銅完全溶解,提起濾紙用約30mL水將上面的溶液沖洗干凈。以高錳酸鉀標準溶液滴定,記錄用量。
1.3.2計算結果
試樣中還原糖質量相當于氧化亞銅的質量,按下式計算:
X0=(V-V0)×c×71.54
式中:
X0 --試樣中還原糖質量相當于氧化亞銅的質量,mg;
V --測定用試樣液消耗高錳酸鉀標準溶液的體積,mL;
V0 --試劑空白消耗高錳酸鉀標準溶液的體積,mL;
C --高錳酸鉀標準溶液的實際濃度,mol/L;
71.54 --1mL高錳酸鉀標準溶液[c(1/5)KMnO4]=1.000mol/L)相當于氧化亞銅的質量,mg。
根據式中計算所得氧化亞銅質量,查表A.1,再計算試樣中還原糖含量(以乳糖計),按下式計算:
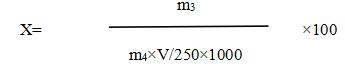
式中:
X --試樣中還原糖的含量, g/100g;
m3 --X0查附錄A之表1得還原糖質量, mg;
m4 --試樣質量或體積, g或mL;
V --測定用試樣溶液的體積 ,mL;
250 --試樣處理后的總體積,mL。
還原糖含量≥10g/100g時,計算結果保留三位有效數字;還原糖含量<10g/100g時,計算結果保留兩位有效數字。
在重復性條件下獲得的兩次獨立測定結果的絕對差值不得超過算術平均值的10%。
1.4結果與討論
1.4.1滴定參數
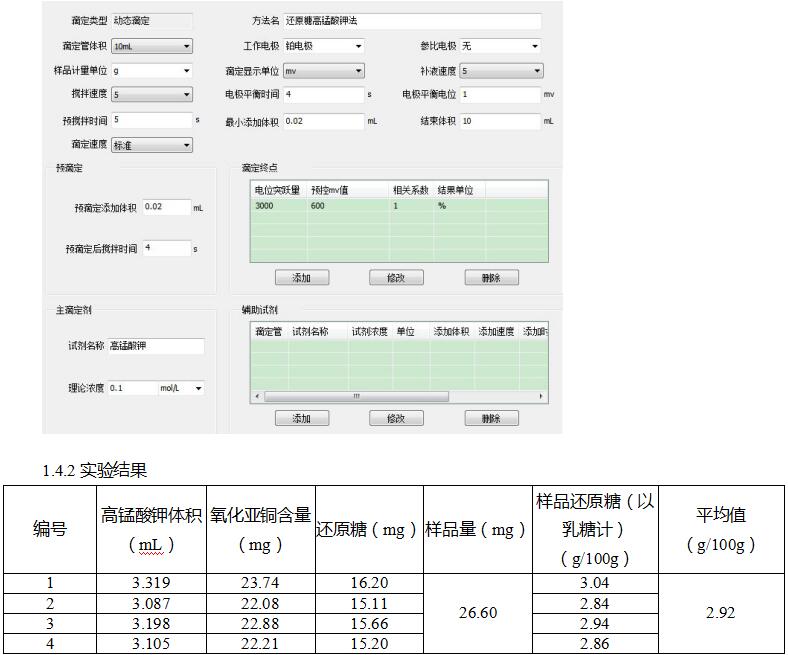
1.4.3曲譜圖
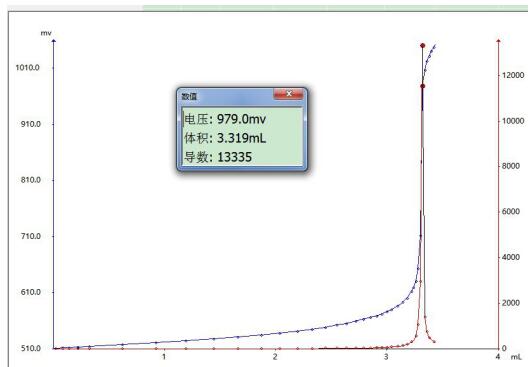
1.4.3討論
實驗精密度要求在重復性條件下獲得的兩次獨立測定結果的絕對差值不得超過算術平均值的10%。經過計算達到國標的要求。
(1)趁熱過濾時需緩慢沿玻棒加入,避免氧化亞銅被沖出濾紙邊緣。
(2)清洗濾紙上的氧化亞銅沉淀時,需仔細翻動濾紙,產生的絮狀碎屑不會影響結果。
(3)仔細沖洗濾紙上的亞鐵離子,以免殘留影響結果重復性。
參考文獻
【1】GB5009.7-2016食品安全國家標準食品中還原糖的測定
【2】GBT 601-2016 化學試劑 標準滴定溶液的制備





