電位滴定法檢測鋅離子的含量
1 實驗原理
在氨性緩沖介質中,以EDTA為滴定劑,Cu-EDTA為置換劑,銅離子選擇電極為指示電極,采用電位滴定法進行滴定。研究表明,Cu-EDTA可增大Zn2+的滴定突躍,提高滴定準確度。
2 實驗儀器
T960電位滴定儀,銅離子選擇電極,10ml滴定管
3 實驗試劑
滴定劑:EDTA標準滴定液(0.02mol/l);PH=10的氨-氯化銨緩沖溶液;0.05mol/l的Cu-EDTA溶液(Cu與EDTA物質的量1:1);氯化鋅溶液
4 實驗步驟
儀器準備,請參照說明書。
取2ml氯化鋅溶液作為被測溶液,加入PH=10的緩沖溶液1.5ml、0.05mol/l的Cu-EDTA溶液3ml、水60ml,在T960電位滴定儀上滴定至終點,同時作空白試驗。
5 實驗數據
1)參數設置

2)實驗結果
C(EDTA)=0.02mol/l
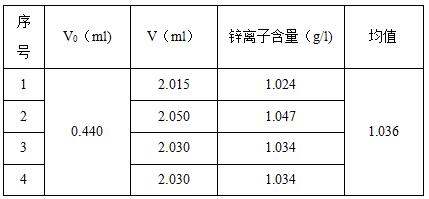
3)滴定圖譜
樣品量:2ml 終點體積:2.015ml
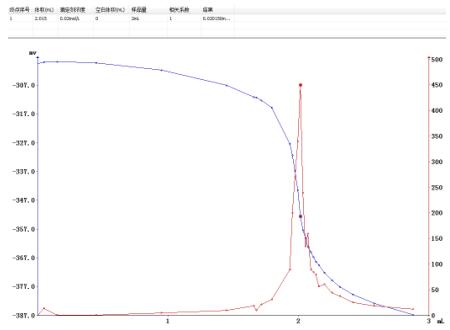
樣品量:2ml 終點體積:2.030ml

6 結論
被測溶液中鋅離子的平均含量為1.036g/l,檢測結果平行性良好。
實驗需注意:氯化鋅易水解,可加少量鹽酸防止水解;經研究發現:加入Cu-EDTA后,Zn2+的滴定突躍明顯增大,因為當加入少量的Cu-EDTA作為置換劑后,Zn2+能置換出Cu2+,而銅離子選擇電極對Cu2+敏感,故可增大突越。加入Cu-EDTA增至3ml以后,突越不明顯,因此Cu-EDTA置換劑選擇加入3ml;當加入的氨性緩沖溶液為1.5ml時,效果最好。
7 參考文獻
中南民族大學學報(自然科學版)-銅離子選擇電極絡合分步滴定鋅和鎂。





