電位滴定法檢測可樂中的還原糖含量
1 前言
還原糖是指具有還原性的糖類,包括葡萄糖、果糖、半乳糖、乳糖、麥芽糖等,是食品檢測的重要指標之一。還原糖常用的測定方法有直接滴定法、高錳酸鉀滴定法和比色法。本文使用電位滴定儀改進了直接滴定法的內容,簡化了操作步驟,避免了顏色判定的誤差,實驗結果重復性良好。
2 儀器與試劑
2.1 儀器

Hanon T960全自動電位滴定儀,
Hamilton高溫鉑復合電極和pH復合電極,
10ml滴定管單元,電陶爐
2.2 試劑
相關配制見附錄。
鹽酸溶液(1+1),堿性酒石酸銅甲液,堿性酒石酸銅乙液,葡萄糖標準溶液(1.0mg/mL) ,硝酸溶液(10%)
3 實驗方法
3.1 實驗步驟
(1)樣品前處理
稱取混勻后的試樣100g(精確至0.01g)于燒杯中,在水浴上微熱攪拌除去二氧化碳后,移入250mL容量瓶中,用水洗滌燒杯,洗液并入容量瓶,加水至刻度,混勻后備用。
(2)堿性酒石酸銅溶液的標定
吸取堿性酒石酸銅甲液5.0mL和堿性酒石酸銅乙液5.0mL,置于滴定杯中。加水10mL,加入葡萄糖標準溶液9.0mL,將電陶爐設為內環火500℃,控制在2min中內加熱至沸,保持沸騰開始滴定至終點,記錄消耗葡萄糖的總體積,同時平行操作3份,取其平均值,計算每10mL(堿性酒石酸甲、乙液各5.0mL)堿性酒石酸銅溶液相當于葡萄糖的質量(mg)。
(3) 試樣溶液預測
吸取堿性酒石酸銅甲液5.0mL和堿性酒石酸銅乙液5.0mL于滴定杯中,加水10mL,將電陶爐設為內環火500℃,控制在2min內加熱至沸,選擇 “動態滴定”模式,保持沸騰用試樣溶液開始滴定至終點,記錄樣液消耗體積。
(4)試樣溶液測定
吸取堿性酒石酸銅甲液5.0mL和堿性酒石酸銅乙液5.0mL,置于滴定杯中,加水10mL,將電陶爐設為內環火500℃,控制在2min內加熱至沸,保持沸騰開始滴定至終點,記錄樣液消耗體積。
3.2 參數設置
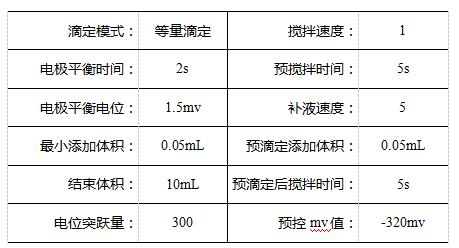
4 結果與討論
4.1 實驗結果
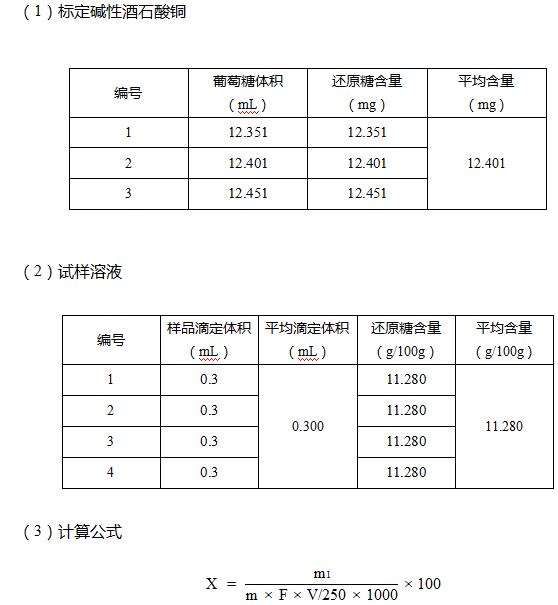
式中:
X --試樣中還原糖的含量(以葡萄糖糖計),單位為克每百克(g/100g);
m1 --堿性酒石酸銅溶液(甲、乙液各半)相當于葡萄糖的質量,單位為毫克(mg);
m --試樣質量,單位為克(g);
F --系數,為1;
V --測定時平均消耗試樣溶液體積,單位為毫升(mL);
250 --定容體積,單位毫升(mL)。
4.2 譜圖
(1)標定堿性酒石酸銅

(2)可樂
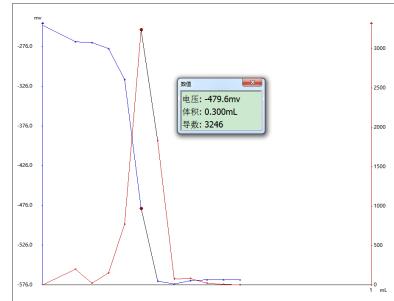
4.3 結論
根據實驗得知,圖譜出現峰值時溶液藍色剛好褪去,且結果符合國標中對于精密度的要求。證實用電位滴定儀采用直接滴定法測定還原糖重復性良好。
參考文獻
[1]GB 5009.7-2016 食品安全國家標準 食品中還原糖的測定[S].
注意事項
1、樣品前處理
水浴蒸發設置溫度為70℃,蒸至攪拌溶液時無氣泡產生,建議提前處理。轉移溶液后將燒杯沖洗3次以上,沖洗液一并移入容量瓶中。
2、堿性酒石酸銅溶液的標定
(1)保持開啟電陶爐500℃的內環火,樣品實際沸騰時間約為90s。
(2)精確移取9.0mL葡萄糖溶液,將帶有攪拌槳、進樣管和鉑復合電極的手動操作臺從滑桿上拿出并扣在滴定杯上,建立并選擇“手動模式”方法,滴加9.0mL葡萄糖溶液。完成后將滴定杯和操作臺一并放在電陶爐上,攪拌并開始計時。
3、試樣溶液測定
(1)預測時儀器方法選擇“動態滴定”,參數同3.2一致。
(2)消耗體積約為0.26mL,所以實際測定時以“手動模式”無需預先加入試樣溶液。
4、滴定管
建議在每次測定前排出滴定管中的氣泡,保證管內充滿液體。
5、清洗電極
建議每次測定后用硝酸溶液(10%)清洗電極鉑環,以保證響應良好。
附錄
1、鹽酸溶液(1+1):量取濃鹽酸50mL,加水50mL混勻;
2、堿性酒石酸銅甲液:稱取無水硫酸銅2.4g和亞甲藍0.0125g,溶于水中,并稀釋至250mL;
3、堿性酒石酸銅乙液:稱取酒石酸鉀鈉12.5g和氫氧化鈉18.75g,溶解于水中,再加入亞鐵氰化鉀1g,完全溶解后,用水定容至250mL,貯存于橡膠塞玻璃瓶中;
4、葡萄糖標準溶液(1.0mg/mL):準確稱取經過98℃~100℃烘箱中干燥2h后的葡萄糖0.5g,加水溶解后加入鹽酸溶液2.5mL,并用水定容至500mL。





